生物医药产业,中国国家发展战略的重要支柱,被国家列为重点发展的战略性新兴产业之一,战略性新兴产业是引导未来经济社会发展的重要力量。在“健康中国2030”规划纲要的指导下,生物医药产业的创新驱动力不断提升,高质量发展将成为生物医药产业的主旋律。长三角各省主要区域都相应出台生物医药产业政策予以扶持。

一、药品研发支持
1.上海市青浦区
(1)临床试验批件。对取得临床试验批件的第1类中药、生物制品、化学药等创新药,完成I、II、III期临床试验,择优按实际投入研发费用的50%分别给予最高不超过200万元、300万元、500万元研发费用补贴。
对取得临床试验批件的第2类中药、生物制品、化学药等创新药,完成I、II、III期临床试验,择优按实际投入研发费用的50%分别给予最高不超过100万元、200万元、300万元研发费用补贴。
需进行临床试验审批的第三类医疗器械,按实际投入研发费用的50%给予最高不超过100万元研发费用补贴。单个企业每年补贴不超过1000万元。
(2)药品注册证书。在本区实施产业化,取得药品注册证书的第1类中药、生物制品、化学药等创新药,给予300万元研发费用补贴;对取得药品注册证书的第2类中药、第2~3类生物制品、第2~4类化学药等改良型新药和仿制药,给予100万元研发费用补贴。对取得批件的兽药,给予50万元研发费用补贴。同一药品不同规格视为同一品种。单个企业每年补贴不超过1000万元。
(3)仿制药一致性评价。支持企业开展仿制药质量和疗效一致性评价,对经国家药监局确定为参比制剂的品种、国内首家通过仿制药质量和疗效一致性评价的品种,给予300万元研发费用补贴;非首家通过仿制药质量和疗效一致性评价的品种,给予100万元研发费用补贴。单个企业每年最高奖励500万元。
(4)生产批件。对关联审评通过的或者单独评审通过的化学原料药、辅料及直接接触药品的包装材料和容器,取得相关资质证书及生产批件、在本区生产且三年内销售额超过2000万元的,给予50万元研发费用补贴。单个企业每年最高不超过200万元。
2.上海市临港新片区
(1)对取得新药药品生产批件和药品上市许可的生物医药企业,每个批件最高给予一次性资助300万元;同一企业最高1000万元。
(2)对第I类化学药、I类生物制品、I类中药及天然药物,按实际投入研发费用的40%予以资助:取得临床批件的,最高不超过800万元资助;完成I、II、III期临床试验的,分别最高不超过1000万、2000万、3000万元,单个企业每年资助最高不超过1亿元。
(3)对第2类化学药、2—5类生物制品、2—6类中药及天然药物,取得临床批件的,给予最高不超过200万元资助;完成I、II、III期临床试验的,分别最高不超过300万、800万、1500万元,单个企业每年资助最高不超过3000万元。
(4)对取得药品批准文号的第3—4类化学药,按实际投入研发费用的20%予以资助,最高500万元;单个企业每年最高1000万元。
(5)对通过仿制药一致性评价的药品,按实际投入研发费用的20%予以资助,最高300万元;单个企业每年资助最高不超过1000万元。
3.江苏省
南京市江宁区:对化学药品1—2类、中药和天然药物1—3类、治疗用生物制品1—5类和预防用生物制品1—3类,获得临床试验批件给予最高100万元资助;完成Ⅰ、Ⅱ、Ⅲ期临床试验,给予150—250万元一次性资助。
苏州市:(1)进入I、II、III期临床试验阶段的新药项目,给予100万元、150万元和250万元一次性资助;完成临床I、II、III期研究的,再按照投入该产品实际研发费用的20%,奖励100—400万元。
(2)对在全国同类仿制药中首个通过一致性评价的药品,按实际投入研发费用的20%予以资助,最高不超过500万元。
泰州市:对完成临床Ⅰ、Ⅱ、Ⅲ期研究的化学药品1类,治疗用生物制品1类和预防用生物制品1类,中药、天然药物1类的新药项目(以下简称“1类新药”),按该产品实际研发费用投入的20%予以奖励,分别给予最高不超过200—650万元一次性奖励。
4.浙江省
萧山区:
(1)进入Ⅱ期、Ⅲ期临床试验研究的,分别给予每项奖励100万元、200万元。
(2)完成Ⅱ期、Ⅲ期临床试验研究的,再按照该项目临床试验发生费用(不含已计入研发经费资助部分)的20%给予资助,最高分别不超过300万元、500万元。
单个项目上述两项临床试验的奖励、资助金额合计不超过该项目临床试验发生费用(不含已计入研发经费资助部分)的30%;单个企业每年获得上述两项临床试验的奖励、资助最高不超过3000万元。获得奖励、资助的项目须在区内实现产业化或销售结算。
(3)获得国家新药注册证书并在区内实现产业化或销售结算的,对单品种累计销售收入首次达到1亿元的,一类新药每个品种给予1000万元奖励,二类和三类新药每个品种给予500万元奖励。
(4)对新通过国家新版药物非临床研究质量管理规范(GLP)、药物(含医疗器械)临床试验质量管理规范(GCP)、中国合格评定国家认可委员会(CNAS)资格认证的生物医药企业给予资助。其中,首次通过GLP认证项目达到三大项、五大项的,分别给予100万元、200万元奖励;取得GCP资格认证的,按每通过1个专业给予10万元奖励并予以累计(含非首次获得GCP认定证书的新增专业),单个企业奖励最高不超过200万元。
(5)在区内取得药品注册批件且实现产业化或销售结算的项目,对于项目总投资(不含研发投入)1亿元以上、5亿元以下的,待项目投产后按项目设备投资额(包括相关软件和技术)的20%予以资助,单个企业资助最高不超过5000万元;项目总投资(不含研发投入)5亿元以上的,待项目投产后按项目设备投资额(包括相关软件和技术)的20%予以资助,单个企业资助最高不超过1亿元。
西湖区:获国家新药注册证书并在本区产业化的一类新药每个品种给予1000万元资助。
宁波市:(1)对1类化学药、1类预防用和治疗用生物制品、中药创新药,按临床试验研究进展给予分阶段后补助。完成临床Ⅱ期按临床试验研究支出的20%、最高不超过1000万元给予后补助(包括临床Ⅰ、Ⅱ期研发费用);完成临床Ⅲ期按临床试验研究支出的20%、最高不超过3000万元给予后补助;取得药品注册证的,再奖励1000万元;单个企业每年后补助最高不超过1亿元。
(2)对2类化学药、2类预防用和治疗用生物制品、中药改良型新药、古代经典名方中药复方制剂,按临床试验研究进展给予分阶段后补助。完成临床Ⅱ期按临床试验研究支出的20%、最高不超过500万元给予后补助(包括临床Ⅰ、Ⅱ期研发费用);完成临床Ⅲ期按临床试验研究支出的20%、最高不超过1000万元给予后补助;取得药品注册证的,再奖励500万元;单个企业每年后补助最高不超过2000万元。
对取得药品批准文号的3-4类化学药、同名同方中药、1-3类兽药注册证,按实际投入研发费用的20%给予后补助、最高不超过500万元;单个企业每年后补助最高不超过1000万元。
金华市:国家新药证书和药品注册批件一类、二类、三类新药给予1000万元资助。
5.安徽省合肥市、亳州市
对在安徽省生产的中药新药(1—4类)及中药经典名方二次开发、化学药新药(1—2类),具有新药证书的生物制品(1—5类)及第三类医疗器械等重大药械项目,对临床前研究按研制费用的20%予以补助,对临床试验按研制费用的10%予以补助,单个项目补助总额最高1000万元。
二、医疗器械研发支持
1.上海市青浦区
(1)医疗器械注册证书。在本区实施产业化,对获得基因测序、肿瘤检测等诊断试剂第三类医疗器械注册证的,给予20万元研发费用补贴;对获得医学影像、植入性组织材料等非诊断试剂第三类医疗器械注册证的,给予50万元研发费用补贴;对获得创新医疗器械第三类医疗器械注册证的,给予100万元研发费用补贴。同一医疗器械不同规格视为同一品种,单个企业每年补贴不超过500万元。
(2)专业资质认证。对药品或医疗器械通过美国食品药品监督局(FDA)、欧洲药品管理局(EMA)、日本药品医疗器械局(PMDA)以及世界卫生组织(WHO)等国际权威认证的,给予100万元奖励。单个企业最高不超过300万元。
2.上海市临港新片区
(1)对临港新片区内取得医疗器械生产许可证的生物医药企业,每个许可证最高给予一次性资助200万元;同一企业年度最高资助500万元。
(2)第二、三类医疗器械产品资助分别最高不超过300、500万元,单个企业每年资助最高不超过1000万元。
2.江苏省
苏州市:对新取得医疗器械注册证书的第三类医疗器械产品,按投入该产品实际研发费用的20%予以资助,最高不超过300万元;对符合第三条所列范围、新取得医疗器械注册证书的第二类医疗器械或其它创新产品,按投入该产品实际研发费用的10%予以资助,最高不超过50万元。单个企业每年资助最高不超过500万元。
泰州市:对落户高新区的影像设备、植介入器械、手术精准定位与导航系统、全降解血管支架、生物再生材料等高端医疗器械及全自动生化分析仪、化学发光免疫分析仪、高通量测序仪、五分类血细胞分析仪等体外诊断设备,按实际研发费用投入20%予以奖励,在取得医疗器械注册证书后,每个品种分别给予不超过300万元一次性奖励。单个企业每年奖励最高不超过1000万元。
3.浙江省
杭州市萧山区:(1)对完成临床试验后并获得CFDA注册受理的第二、三类医疗器械,具有自主知识产权并在区内实现产业化或销售结算的,根据实际临床试验发生费用(不含已计入研发经费资助部分)和注册费用合计的50%进行资助,每个产品最高不超过100万元。对进入创新医疗器械特别审批或优先审评程序的,根据实际临床试验发生费用(不含已计入研发经费资助部分)和注册费用合计的50%进行资助,每个产品最高不超过200万元。单个企业每年资助合计最高不超过1000万元。
(2)在区内取得创新型二类、三类医疗器械注册证且实现产业化或销售结算的项目,对于项目总投资(不含研发投入)5000万元以上、1亿元以下的,待项目投产后按项目设备投资额(包括相关软件和技术)的20%予以资助,单个企业资助最高不超过1000万元;项目总投资(不含研发投入)1亿元以上、5亿元以下的,待项目投产后按项目设备投资额(包括相关软件和技术)的20%予以资助,单个企业资助最高不超过5000万元;项目总投资(不含研发投入)5亿元以上的,待项目投产后按项目设备投资额(包括相关软件和技术)的20%予以资助,单个企业资助最高不超过1亿元。
宁波市:对取得二类、三类医疗器械注册证书产品(含免疫发光试剂,不含其他二类诊断试剂)并在我市产业化的,按单品种实际投入研发费用的20%分别给予最高不超过200万元、500万元后补助;获得创新二类、三类医疗器械注册证的,单品种分别再给予一次性研发费用奖励100万元、300万元。
金华市:首次获得医疗器械注册证的产品予以1000万元资助。
4.安徽省合肥市、亳州市
对纳入目录、经评审认定符合条件医疗器械的首次应用,对省内研制单位按售价10%予以补助,最高500万元。
三、医疗项目支持
1.上海市青浦区
(1)对生物医药制造业企业年度产值首次突破1亿元、5亿元、10亿元、20亿元、50亿元的企业,分别给予10万元、50万元、100万元、200万元、500万元奖励。
(2)对生物医药研发服务业企业年度主营业务收入首次突破5000万元、1亿元、2亿元、5亿元、10亿元的企业,分别给予5万元、10万元、20万元、50万元、100万元奖励。
(3)对药品批发和医疗器械经营许可企业,运行一年以上经营收入首次突破10亿元、20亿元、50亿元、100亿元的,分别给予20万元、40万元、100万元、200万元奖励。
2.上海市临港新片区
支持对临港新片区生物医药产业发展具有全局带动和重大引领作用的产业项目建设,按照项目总投资的10%—30%比例给予支持,最高支持金额不超过5亿元。
2.江苏省苏州市
(1)在苏州项目总投资1亿元以上,5亿元以下的,按实际投入的10%予以资助,每个企业资助最高不超过2000万元;项目总投资5亿元以上的实行“一事一议”。
(2)对于获得重大新药创制国家、省级科技重大专项的项目,按照项目资金的20%进行资助,最高不超过2000万元。
(3)取得第二、三类医疗器械注册证,且在苏州大市范围内实施产业化的项目,对于项目总投资5000万元以上,1亿元以下的,按实际投入的10%予以资助,每个企业资助最高不超过500万元;项目总投资1亿元以上的实行“一事一议”。
(4)运用工业互联网、大数据、人工智能等技术对现有生产设施、工艺装备进行技术改造的优秀项目,经评审分类分等级,最高按照项目投资额的15%予以资助,单个企业每年资助最高不超过500万元。
3.浙江省
金华市:项目固投金额3亿元以上的,自项目投产之日起第1年至第5年按开发区综合贡献额一定比例给予奖励。
杭州市:企业申报国家级科技计划项目,验收通过后按1:1给予配套资助,最高不超过1500万元。
4.安徽省合肥市、亳州市
(1)支持健康医疗大数据中心、超算中心、干细胞库、中药材大数据中心、转化医学研究中心、活细胞成像平台等重大医疗医药创新发展基础能力建设,对经评审认定的项目,按照关键设备投资的10%予以补助,最高2000万元。
(2)加快推进肿瘤免疫治疗、细胞治疗、再生医疗等现代医疗技术创新及临床应用,对经评审认定具备承担条件的项目,按照科研攻关和应用推广发生费用的30%予以资助,最高500万元。
四、医药、医疗平台支持
1.上海市青浦区
(1)对医药合同研发机构(CRO)、医药合同外包生产机构(CMO)、医药合同定制研发生产机构(CDMO)等产业应用基础平台,以及实验动物服务平台、检验检测平台、临床试验机构、非临床安全性评价研究机构等产业公共服务平台,按照认定的固定资产投资额的20%给予资助,最高500万元。
(2)支持公共服务平台为本区生物医药企业提供服务,每年按实际服务金额的10%予以资助,单个平台每年资助最高不超过100万元。
2.上海市临港新片区
(1)加快培育引进行业龙头合同研发机构(CRO)、合同外包生产机构(CMO)、合同定制研发生产机构(CDMO)等生物医药产业专业技术平台,按项目总投资的50%予以资助,最高不超过5000万元。
(2)药物及医疗器械第三方检测服务、GMP共性实验室、实验动物服务、药物筛选、药理毒理研究、成效性评价、新药报批、医药工业废弃物处理等公共服务平台,按照项目总投资的50%比例给予支持,支持金额不超过3000万元。
(3)支持企业、高校、相关机构协同合作建设临床医学研究中心,开展国际多中心临床试验、建设临床样本资源库、健康大数据平台、药物和医疗器械临床评价平台。按照项目总投资的50%比例给予支持,支持金额不超过3000万元。
2.江苏省苏州市
(1)对于在生物医药产业重点区域新建的药物非临床安全性评价机构、药物(含医疗器械)临床试验机构、有特殊专业要求的临床研究医院、生物医药产业中试及生产平台、专业孵化器、实验动物服务平台、检验检测平台、生物大分子筛选平台、转化医学研究中心、医疗大数据临床研究应用中心、精准医学研究中心、合同定制研发生产服务机构(CDMO)、生物医药物流平台、医药工业废弃物处理设施等公共服务平台,经认定后按照项目总投资的30%予以最高不超过2000万元的资助。
(2)对于已建成运营的生物医药产业公共服务平台,经认定后,按照其上年度为苏州市企业(与本机构无投资关系)服务金额的10%予以资助,每年最高不超过500万元。
(3)对苏州市生物医药领域组建的产业创新中心等专业服务机构,按照国家级、省级、苏州市级不同等次分别给予2000万元、1000万元和500万元的一次性资助,用于相关机构开展重大产业项目引进、创新平台规划建设、孵化器培育等工作。
3.浙江省
杭州市萧山区:(1)经评定且符合区内规划的生物医药公共服务平台,按其购置研发设备总价的50%给予资助,最高不超过3000万元。
(2)区内GLP、GCP、生物医药研发外包(CRO)、生物医药研发生产外包(CDMO)、生物医药产业中试平台等研发服务机构,为与其无投资关系的区内生物医药企业提供服务的,给予年度合同实际金额的5%、单个机构每年最高不超过500万元的奖励
宁波市:药物研发服务平台、实验动物平台、检验检测平台、生物医药产业中试及生产平台、GMP(药品生产质量管理规范)共性工厂等产业公共服务平台。经国家资质认定的,按其总投资的30%给予补助,最高不超过2000万元。
宁波市:支持建设药物研发服务平台、实验动物平台、检验检测平台、生物医药产业中试及生产平台、GMP共性工厂等产业公共服务平台;经国家资质认定的,按照总投资的30%给予补助、最高不超过2000万元。对于总投资超过5亿元的平台建设项目,给予“一事一议”扶持政策。
4.安徽省合肥市、亳州市
支持现代医疗和医药企业、科研院所建设重点实验室、工程研究中心等创新平台,按照支持“三重一创”建设政策规定予以支持。(牵头单位:省发展改革委;配合单位:省科技厅、省财政厅)对临床医学研究中心的建设单位,以科研项目、平台建设、人才培养、国际合作、重点学科建设等多种形式予以支持。
五、医疗人才支持
1.上海市临港新片区
享受临港新片区人才政策,如紧缺急需人才、紧缺急需技能人才、高等级技能人才、特殊人才可直接落户;各类其他人才享受居住证专项加分、“居转户”年限缩短。
2.江苏省
苏州市:深化完善姑苏创新创业领军人才计划,取消申报人年龄限制,放宽学历要求。对生物医药产业领军人才,给予100—400万元项目资助和100—250万元安家补贴。加大对生物医药企业引进重点产业紧缺人才的支持力度,给予6—12万元薪酬补贴。对生物医药企业通过中介机构猎头引进产业领军人才的,给予每年最高100万元佣金补贴。对引进创新领军人才的生物医药企业,给予最高50万元引才奖励。为生物医药等产业人才开辟职称评审绿色通道,符合条件的可直接授予相应职称。加强人才乐居保障,对符合条件的生物医药产业顶尖人才给予最高500万元购房补贴,按照人才对地方的贡献,给予最高100万元贡献奖励。完善高层次人才“一站式”服务体系,为符合条件的生物医药产业人才提供人才落户(含外籍人才永久居留证)、医疗保障及子女教育等优惠待遇。
泰州市:对于知名国际医疗机构、国内一流或顶尖医疗机构(医生团队)可享受“一事一议”政策。对于能够瞄准医学前沿、提供以先进医疗技术为特色的医疗服务,其学科能够填补全省临床医疗专科空白的三级甲等医院实行“一院一策”政策。
3.浙江省杭州市萧山区
实际投入达5000万元(含)以上的生物医药企业,参照区内总部经济对高级管理人员的政策扶植力度,对其不超过10名高级管理人员和技术专家给予支持。
4.安徽省合肥市、亳州市
用好现有人才资源,加大现代医疗和医药产业高层次创新人才引进、培养和创新团队建设力度,健全激励机制。共建中国科学技术大学生命科学与医学部,培养医学高端人才。支持安徽医科大学、安徽中医药大学等高等院校创新发展现代医疗和医药类学科,探索专业人才定向培养模式,加强专业技术人才培训工作。鼓励市县创新支持方式集聚一批高水平现代医疗和医药人才队伍。
生物医药产业是关系国计民生的特殊朝阳产业,覆盖范围广、产业链条长、增长潜力大。目前,长三角生物医药产值接近全国的30%,拥有一批国内领军企业,是长三角地区最具竞争力的优势产业之一。
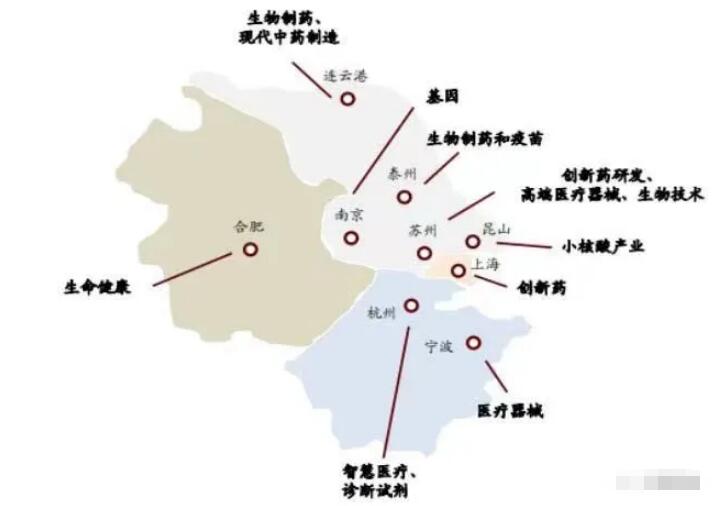
长三角地区拥有国内最多的跨国生物医药企业,在研发与产业化、外包服务、国际交流等方面具有较大优势。同时,长三角地区通过龙头企业布局、园区共建、监管政策统一等推动生物医药产业协同发展。
上海作为龙头,人才、科研院所与研发机构、大实验装置、临床资源、创新平台、国际联系等创新链环节优势突显,形成了完善的生物医药创新体系和产业集群;江苏具有全国最强的产业化优势,并且初步形成各地特色优势,如苏州的创新药、泰州的生物制药和疫苗、昆山的小核酸、南京的基因产业等;浙江发挥生产制造与数字经济融合优势,形成以杭州国家生物产业基地和台州国家化学原料基地为核心的产业格局。安徽中医药特色突出。
声明:转载目的在于传递更多信息,并不代表赞同其观点和对其真实性负责。文字、图片版权均属权利人,如涉及作品内容、版权和其它问题,请及时与我们联系。
